
L’autèntica memòria de l’aigua: els isòtops estables
-
- Home
-
- 1 of 1
Aquell que no estigui avesat a la física nuclear, si sent el mot isòtop pensarà en la radioactivitat, o en l’equip de futbol americà de Springfield, la ciutat fictícia dels Simpson. Si més no, això era el que em venia al cap fins que començant la tesi doctoral vaig conèixer la Monica Mejía-Chang, que em va introduir en el món dels isòtops estables. Tot i que els radioactius s’enduen la fama, els isòtops estables són molt més comuns.
Els elements de la taula periòdica estan definits pel nombre de protons del nucli atòmic (nombre atòmic). La majoria d’elements pot presentar un nombre diferent de neutrons al nucli encara que tinguin el mateix nombre atòmic, i això produeix lleugeres diferències en la massa atòmica. Així doncs, dos àtoms d’un mateix element químic (amb el mateix nombre atòmic) que tinguin un nombre diferent de neutrons són el que anomenem isòtops. Aquests poden ser estables o radioactius. Per exemple, l’hidrogen té dos isòtops estables, l’hidrogen 1 i l’hidrogen 2 (el número fa referència a la suma del nombre de protons i neutrons), i a més a més, té també un isòtop radioactiu, l’hidrogen 3, que emet radiació a mesura que es desintegra. Una molècula d’aigua que contingui només hidrogen-1 serà més lleugera que no pas una que només contingui hidrogen 2, i això, com veurem, té conseqüències. En propers articles, parlaré de com els isòtops de l’aigua s’utilitzen en les ciències ambientals, concretament en l’ecohidrologia, la climatologia i l’ecofisiologia, però també en l’arqueologia o les ciències forenses. En aquest article, presento alguns dels principals conceptes i processos fisicoquímics que regeixen l’aplicació dels isòtops estables de l’aigua en totes aquestes disciplines científiques.
Els isòtops estables a l’aigua
L’abundància a la Terra dels isòtops estables és sovint desequilibrada. En el cas de l’oxigen, l’isòtop més comú és l’oxigen 16 (99,76%), seguit de l’oxigen 18 (0,2%) i el raríssim oxigen 17 (0,038%). El mateix passa amb l’hidrogen 1 (99,98%) i l’hidrogen 2 (0,015%) (Figura 1a). Les molècules d’aigua tenen per tant diferents isotopòlegs, que són versions de la mateixa molècula, però amb diferent composició isotòpica (Figura 1b). Més enllà dels tecnicismes, el fet rellevant és que per molt que s’assemblin dues gotes d’aigua, l’anàlisi de la composició isotòpica ens permet diferenciar-les i fins i tot, seguir-ne el destí. A més a més, la composició isotòpica també ens pot il·lustrar sobre l’origen geogràfic de l’aigua i sobre quins processos fisicoquímics ha patit.
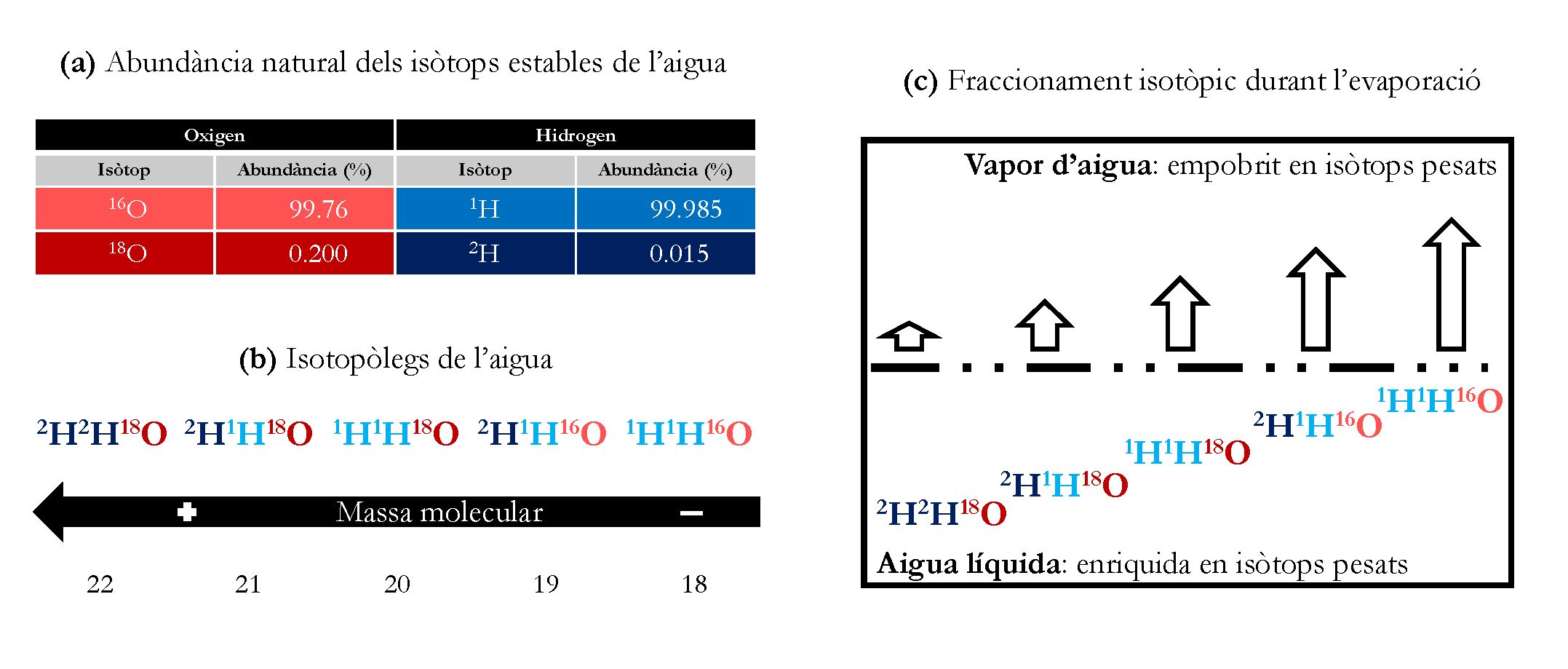
Figura 1. Esquema conceptual dels isòtops estables de l’aigua. S’hi mostren alguns dels isotopòlegs de l’aigua de diferent massa molecular. Font: Elaboració pròpia.
El fenomen que permet l’aplicació de la composició isotòpica de l’aigua en estudis de diverses disciplines científiques és el fraccionament isotòpic. Durant els canvis d’estat de l’aigua, les molècules més lleugeres (amb isòtops oxigen 16 i hidrogen 1) tindran una tendència major que les més pesades a passar de l’estat líquid al gasós (evaporació). En canvi, durant el pas de gas a líquid (condensació), les molècules més pesades tindran una major tendència a canviar d’estat (Figura 1c). Així, el fraccionament isotòpic de les molècules d’aigua fa que el vapor atmosfèric tingui una composició isotòpica més lleugera que la massa d’aigua on s’ha originat, sigui l’oceà, un llac o la transpiració de les plantes.
De la mateixa manera, podem dir que les molècules d’aigua tenen memòria. Però compte, no en el sentit que li donen els homeòpates. Si agaféssim una ampolla d’un litre d’aigua, n’evaporéssim la meitat i féssim condensar completament el vapor resultant en una ampolla exactament igual a l'original, mesurant-ne la composició isotòpica es podria saber quina és l’ampolla original, i quina conté l’aigua evaporada i després condensada. I és que el mig litre d’aigua que no s’ha evaporat contindria una major proporció dels isòtops pesats, amb menys tendència a evaporar-se que no pas els lleugers.
A escala global, els cicles d’evaporació i condensació de l’aigua determinaran la composició isotòpica de la precipitació, i aquesta, la de rius i llacs, els aqüífers, la humitat del sòl i l’aigua absorbida per les arrels. A més a més, la temperatura té un efecte important en el fraccionament isotòpic, ja que en determina la intensitat. A temperatures altes, la tendència d’evaporació (o condensació) dels diferents isòtops no és tan diferent com quan la temperatura és baixa. És a dir, l’aigua no només "memoritza" els canvis d’estat que ha patit, sinó que també ens pot informar de la temperatura que hi havia durant aquests canvis d’estat.
Composició isotòpica de la precipitació: processos i patrons espaciotemporals
L’any 1964, el paleoclimatòleg danès Willi Dansgaard publicà un article a la revista Tellus titulat “Els isòtops estables en la precipitació”,1 on descrivia amb gran detall tots els processos físics i químics que determinen la composició isotòpica de l’aigua meteòrica, és a dir, l’aigua que precipita en estat líquid (pluja i boira) o sòlid (neu i calamarsa). D’aquests processos, el més important és la condensació, durant la qual els isòtops més pesats del vapor atmosfèric condensen en gotes d’aigua amb més facilitat que no pas els més lleugers. Com s’ha dit, l’aigua que precipita serà més enriquida en els isòtops pesats (oxigen 18 i hidrogen 2) que no pas el vapor d’on s’ha originat. Donat que la temperatura té efectes en la intensitat del fraccionament isotòpic, aquests processos variaran en funció del clima.
Harmon Craig (1961)2 va formalitzar que les proporcions dels isòtops pesats de l’hidrogen (δ2H) i l’oxigen (δ18O) a les aigües meteòriques de tot el món guarden una relació lineal amb pendent igual a 8 (Figura 2). La precipitació d’indrets càlids se situa a la part més positiva (aigua més pesada) de la recta, i la d’indrets més freds a la part més negativa (aigua més lleugera).
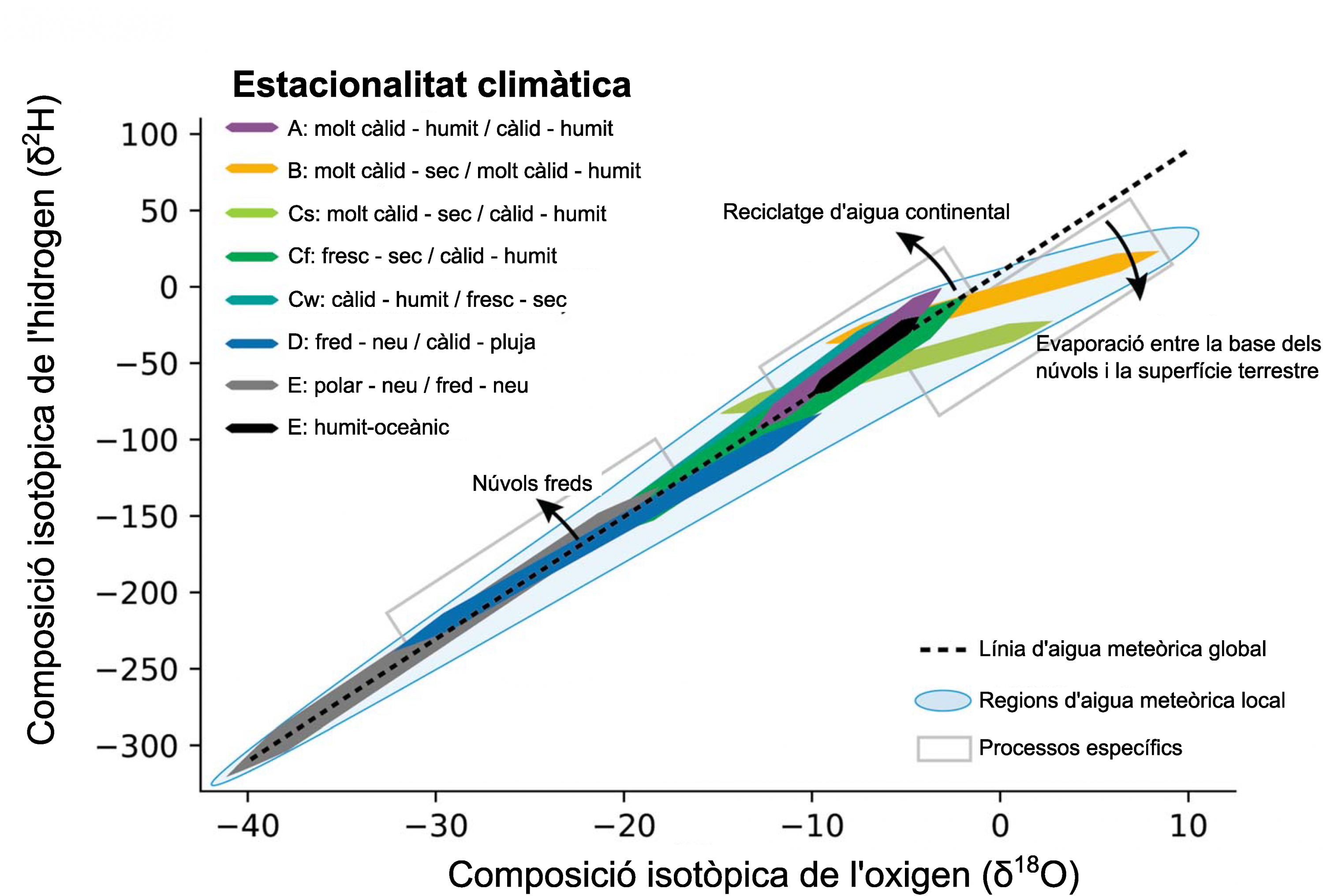
Figura 2. Relació entre la composició isotòpica de la precipitació (δ18O i δ2H) en zones de diferent estacionalitat climàtica (diferent color). A la llegenda s’hi detallen les dues estacions principals de cada clima. La línia discontínua correspon a la línia global de les aigües meteòriques, i s’hi mostren els efectes isotòpics d’alguns processos atmosfèrics. Font: Adaptat de Putnam et al.3
Si donem un cop d’ull al mapa global de la composició isotòpica mitjana anual de la precipitació (Figura 3), s’observa clarament que en climes freds de latituds boreals la precipitació és molt més empobrida en isòtops pesats que no pas en els climes tropicals (valors negatius de δ18O indiquen una menor proporció de 18O en relació amb l’estàndard, que és l’aigua oceànica, el mateix és vàlid per a δ2H).
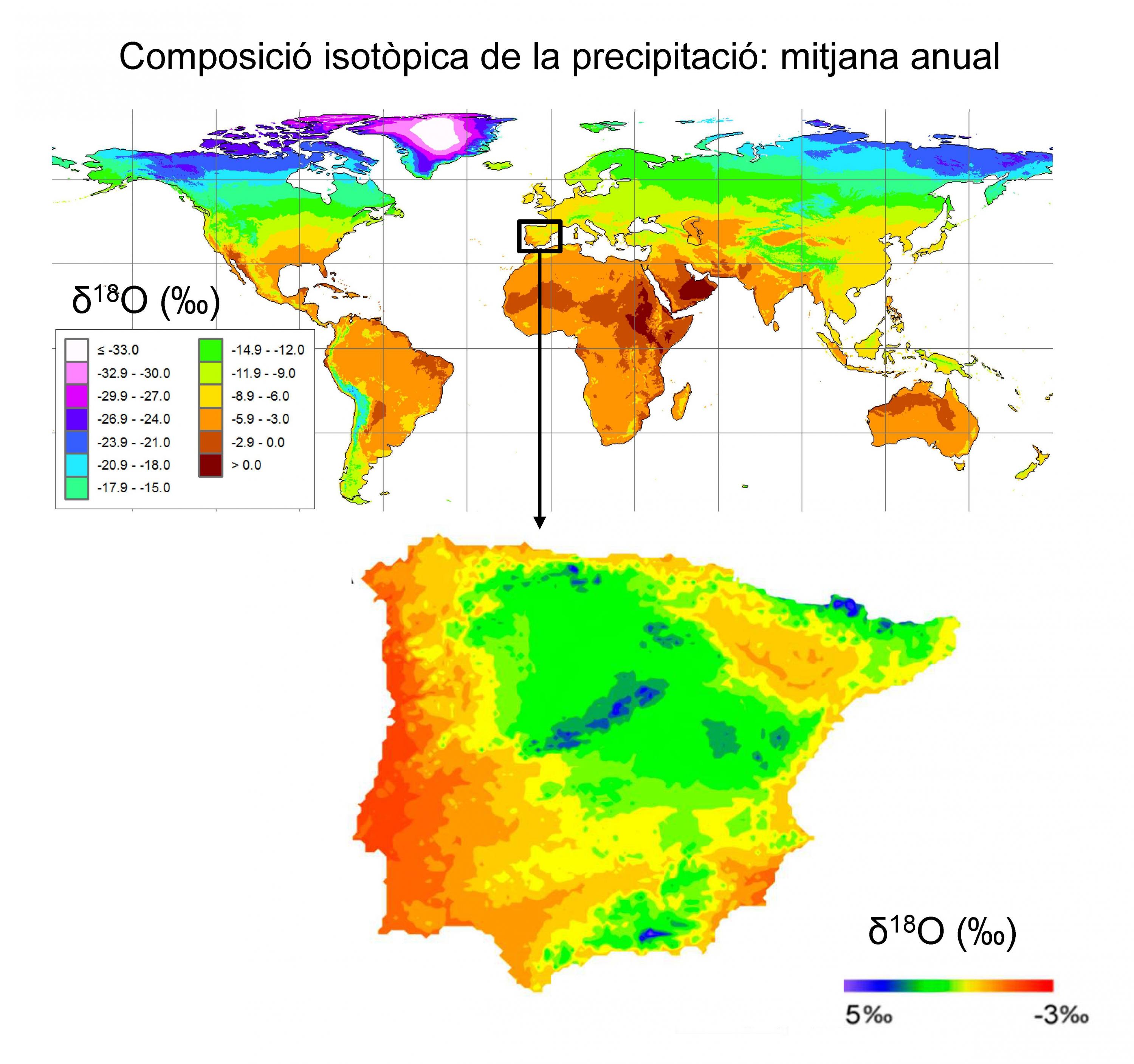
Figura 3. Patrons geogràfics de la composició isotòpica de la precipitació, mitjana ponderada a escala global (mapa superior) i per a la península Ibèrica durant el període octubre 2004-juliol 2006 (mapa inferior), adaptats de Terzer et al.4 i Hatvani et al.,5 respectivament. Cada mapa té una escala i llegenda diferents.
Per entendre els processos que determinen la composició isotòpica de la precipitació, podem dividir els seus efectes entre temporals i espacials.
Els efectes temporals impliquen que, en un mateix indret, les condicions atmosfèriques de cada episodi de precipitació en determinaran la composició isotòpica. En la Figura 4 es mostra la composició isotòpica de la precipitació al llarg d’onze anys a Cestàs, localitat de la Gironda (SO de França), dividida en estacions climàtiques. La pluja (o rarament la neu) d’hivern és més pobra en isòtops pesats (valors negatius de δ), la pluja estival és més enriquida en isòtops pesats (valors positius de δ), mentre que a la tardor i la primavera la pluja pren valors intermedis de δ. Aquestes diferències isotòpiques estacionals són causades principalment per la temperatura. Cestàs és molt a prop de l’oceà Atlàntic i per tant les variacions tèrmiques són molt moderades (grup “Cf” en la Figura 2). En climes més continentals, veuríem patrons estacionals dels isòtops de la precipitació molt més marcats.
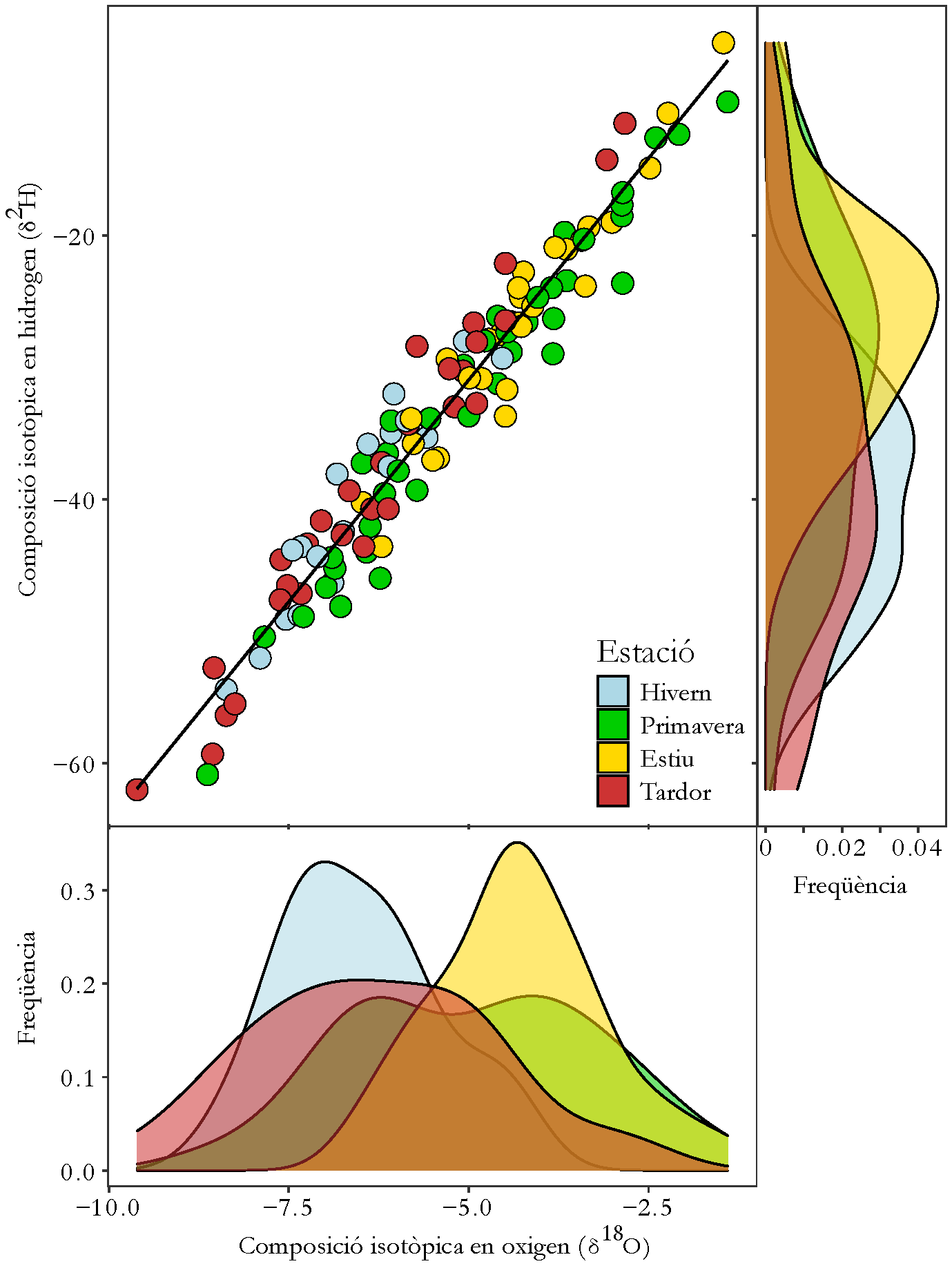
Figura 4. Composició isotòpica de la precipitació a Cestàs (França) en diferents estacions meteorològiques per al període 2005-2016. A més dels valors mensuals de δ18O i δ2H, també s'hi mostra la distribució dels valors per estació (freqüència). Font: Elaboració pròpia.
Un altre factor que intervé en la variació estacional de la composició isotòpica de la pluja és l’origen del vapor atmosfèric. Per exemple, a Catalunya, les masses d’aigua que s’han evaporat a l’Atlàntic Nord tenen una composició isotòpica més lleugera que les que provenen del mar Mediterrani6, ja que l’evaporació és més forta al Mare Nostrum, i les capes superficials del mar són sempre més enriquides en els isòtops més pesats. Com que l’origen de les pluges també varia estacionalment, aquest es veurà reflectit en la composició isotòpica de la pluja.
Tot i que a gairebé tot arreu es poden apreciar diferències estacionals en la composició isotòpica de la precipitació, les característiques geogràfiques de cada indret dominaran els valors mitjans a escala anual. Els efectes espacials són per tant molt rellevants, ja que més enllà de la massa d’aigua on el vapor s’origina, les masses d’aire humit estan permanentment sotmeses a processos de fraccionament. Les masses d’aire humit perden preferentment els isòtops pesats a través de la condensació. Si pensem en un front atlàntic que comença a produir precipitacions a Portugal, primer aniran perdent relativament més els isòtops pesats, i per tant, si arriba a València i encara produeix precipitació, aquesta estarà empobrida en isòtops pesats. La temperatura mitjana de València és més càlida que la de Porto, i per tant, esperaríem trobar més isòtops pesats en la pluja de la ciutat mediterrània. Tot i això, com que la direcció dominant de les masses d’aire és d’oest a est, trobem que la precipitació a València, de mitjana, és més empobrida en els isòtops pesats que no pas la de Porto (Figura 3)7. Això és en part degut al progressiu empobriment que pateix l’aigua atmosfèrica a mesura que travessa la península Ibèrica.
L’orografia també té un efecte important en els patrons espacials de la composició isotòpica de la precipitació. Quan una massa d’aire humit topa amb un massís muntanyós i produeix precipitació, a mesura que s’enfila pels vessants haurà anat perdent, primer, els isòtops pesats, i així, la precipitació a les zones més elevades estarà més empobrida en isòtops pesats8 (Figura 5). Per aquest motiu, la precipitació de Sierra Nevada és molt més empobrida en isòtops pesats que la de qualsevol punt de la costa cantàbrica (Figura 3). A més a més, processos atmosfèrics com els núvols freds, que contenen aigua en estat líquid i sòlid, el reciclatge d’aigua evaporada de la superfície terrestre i l’evaporació que pateix la precipitació des de la base dels núvols fins que precipita a la superfície, també exerceixen efectes isotòpics que són quantificables i observables en desviacions de la relació lineal dels isòtops de l’oxigen i l’hidrogen (Figura 2).
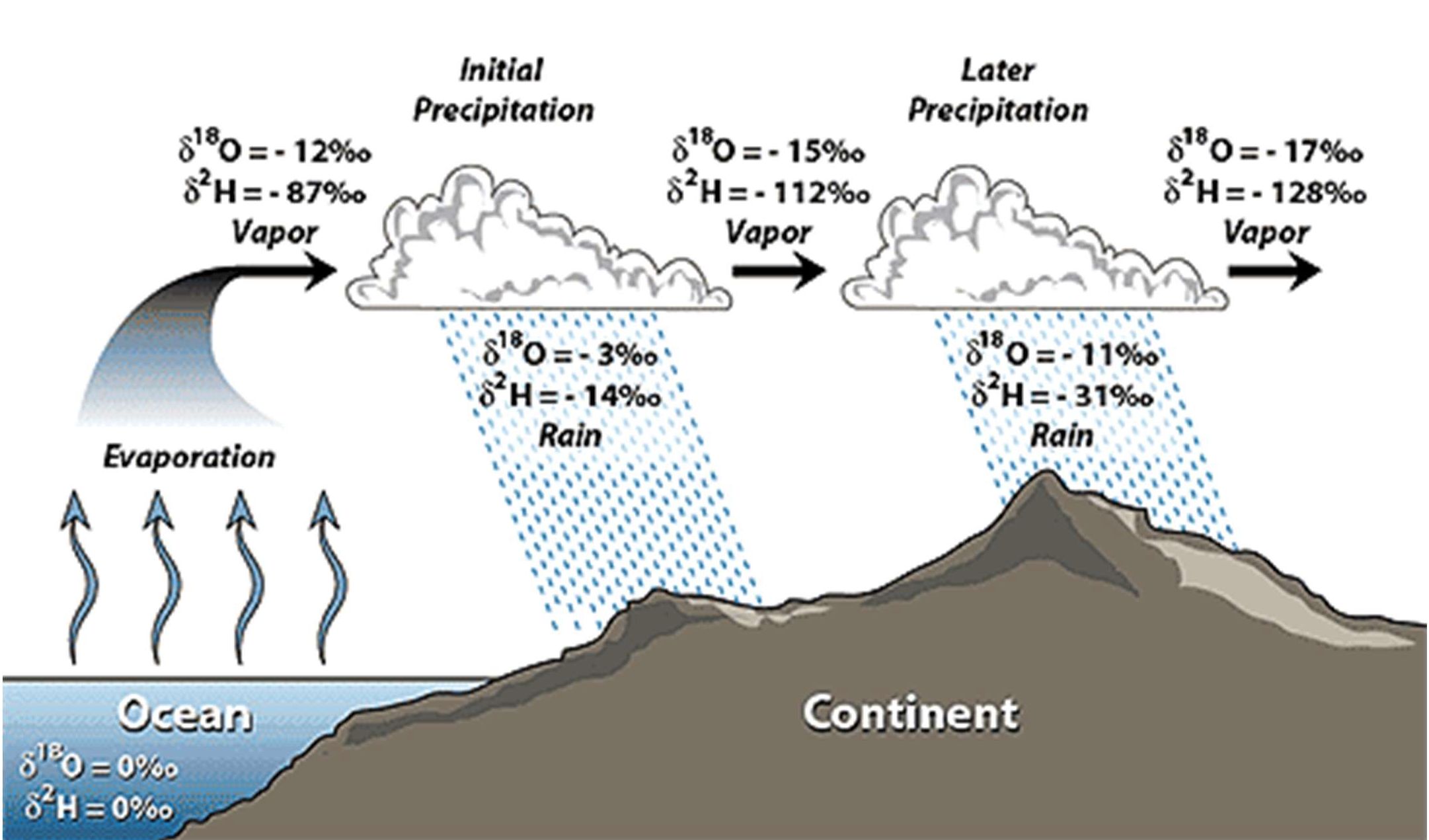
Figura 5. Esquema conceptual dels efectes isotòpics de les masses d’aire humit des que s’originen a l’oceà fins que precipiten al continent. Font: Adaptat per SAHRA (http://web.sahra.arizona.edu/) i basat en Hoefs9 i Coplen et al.10
El coneixement acumulat sobre els processos naturals que modifiquen la composició isotòpica de l’aigua té moltes aplicacions. Sovint, és la mateixa aplicació la que ha desencadenat, per pur atzar, descobriments sobre processos de fraccionament isotòpic que després són integrats dins el marc teòric per comprendre millor la dinàmica dels fluxos d’aigua a escala planetària, regional, d’ecosistema, d’organisme i fins i tot de teixit biològic. De fet, per ser exactes hauríem d’incloure també l'àmbit extraplanetari, ja que els isòtops de l’aigua també s’han utilitzat per indagar sobre l’origen de l’aigua lunar11 i la formació d'aquest astre.12
Referències
1. Dansgaard, W. "Stable isotopes in precipitation". Tellus 16, 436–468 (1964).
2. Craig, H. "Isotopic Variations in Meteoric Waters". Science 133, 1702—1703 (1961).
3. Putman, A. L., Fiorella, R. P., Bowen, G. J. i Cai, Z. "A Global Perspective on Local Meteoric Water Lines: Meta-analytic Insight Into Fundamental Controls and Practical Constraints". Water Resour. Res. 55, 6896–6910 (2019).
4. Terzer, S., Wassenaar, L. I., Araguás-Araguás, L. J. i Aggarwal, P. K. "Global isoscapes for δ18O and δ2H in precipitation: Improved prediction using regionalized climatic regression model"s. Hydrol. Earth Syst. Sci. 17, 4713–4728 (2013).
5. Hatvani, I. G., Erdélyi, D., Vreča, P. i Kern, Z. "Analysis of the spatial distribution of stable oxygen and hydrogen isotopes in precipitation across the Iberian Peninsula". Water 12, (2020).
6. Celle-Jeanton, H., Travi, Y. i Blavoux, B. "Isotopic typology of the precipitation in the Western Mediterrenean region at the three different time scales". Geophys. Res. Lett. 28, 1215–1218 (2001).
7. Araguas-Araguas, L. J. i Diaz Teijeiro, M. F. Isotope composition of precipitation and water vapour in the Iberian peninsula. (2005).
8. Liotta, M., Favara, R. i Valenza, M. "Isotopic composition of the precipitations in the central mediterranean: Origin marks and orographic precipitation effects". J. Geophys. Res. Atmos. 111, 1–12 (2006).
9. Hoefs, J. Stable isotope geochemistry(Eighth Edition). Springer International Publishing vol. 43 (2019).
10. Coplen, T. B., Herczeg, A. L. & Barnes, C. "Isotope Engineering-Using Stable Isotopes of the Water Molecule to Solve Practical Problems". En Environmental Tracers in Subsurface Hydrology (2000). doi:10.1007/978-1-4615-4557-6_3.
11. Greenwood, J. P. et al. "Hydrogen isotope ratios in lunar rocks indicate delivery of cometary water to the Moon". Nat. Geosci. 4, 79–82 (2011).
12. Robinson, K. L. & Taylor, G. J. "Heterogeneous distribution of water in the Moon". Nat. Geosci. 7, 401–408 (2014).





