
Un enllaç metàl·lic en una molècula de sis àtoms
-
- Home
-
- 8 of 11
L'enllaç químic és sens dubte el concepte més fonamental de la química. Una reacció química no és més que el trencament d'enllaços químics existents i la formació de nous enllaços químics. El concepte d'enllaç químic s'introdueix en els primers cursos de química. En aquests cursos s'aprèn que l'enllaç químic en les molècules pot ser covalent o iònic i que en els metalls tenim l'enllaç metàl·lic. En aquest enllaç metàl·lic, els nuclis, juntament amb els electrons més interns, formen partícules carregades positivament que estan distribuïdes de forma simètrica en el cristall. Els electrons de valència es troben deslocalitzats en el que es considera un mar d'electrons al voltant de les partícules carregades positivament. Aquests electrons lliures són els responsables que els metalls presentin una elevada conductivitat elèctrica i tèrmica. Recentment, investigadors de l'Institut de Química Computacional i Catàlisi de la Universitat de Girona, en col·laboració amb investigadors del Donostia International Physics Center (DIPC) i de la Universitat de Melbourne, han publicat en el Chem. Eur. J. el cas d'una molècula d'únicament sis àtoms enllaçats per un enllaç químic de les mateixes característiques que el dels metalls. Es tracta de la molècula de simetria octaèdrica Li6+ amb un espín de 3/2 (és a dir, amb tres electrons desaparellats) i una distància Li-Li d'aproximadament 3 À. Cada àtom de Li amb una configuració 1s22s1 contribueix amb un electró de valència i per tant la molècula té cinc electrons de valència. La resta són electrons interns que es troben molt propers al nucli de cada àtom. Els cinc electrons de valència ocupen els orbitals moleculars que es mostren a la figura següent:
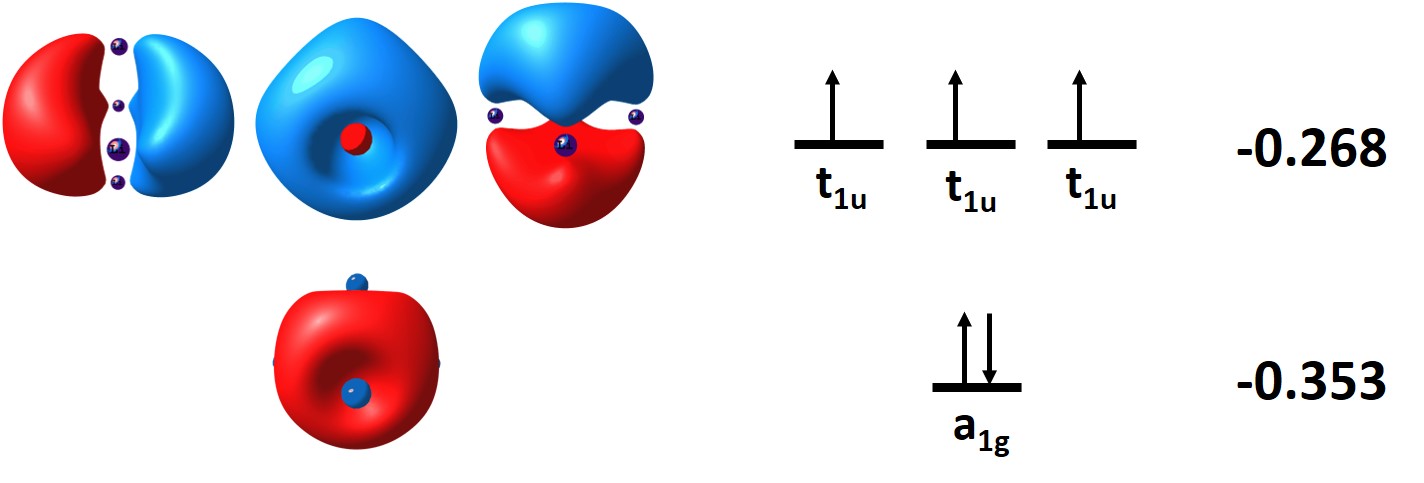
La química teòrica disposa de diverses eines per determinar on es localitzen els electrons en les molècules. Una d'aquestes eines és la funció de localització electrònica (ELF). La gràfica d'aquesta funció, en el cas del 3/2Li6+, és la que es mostra a continuació:
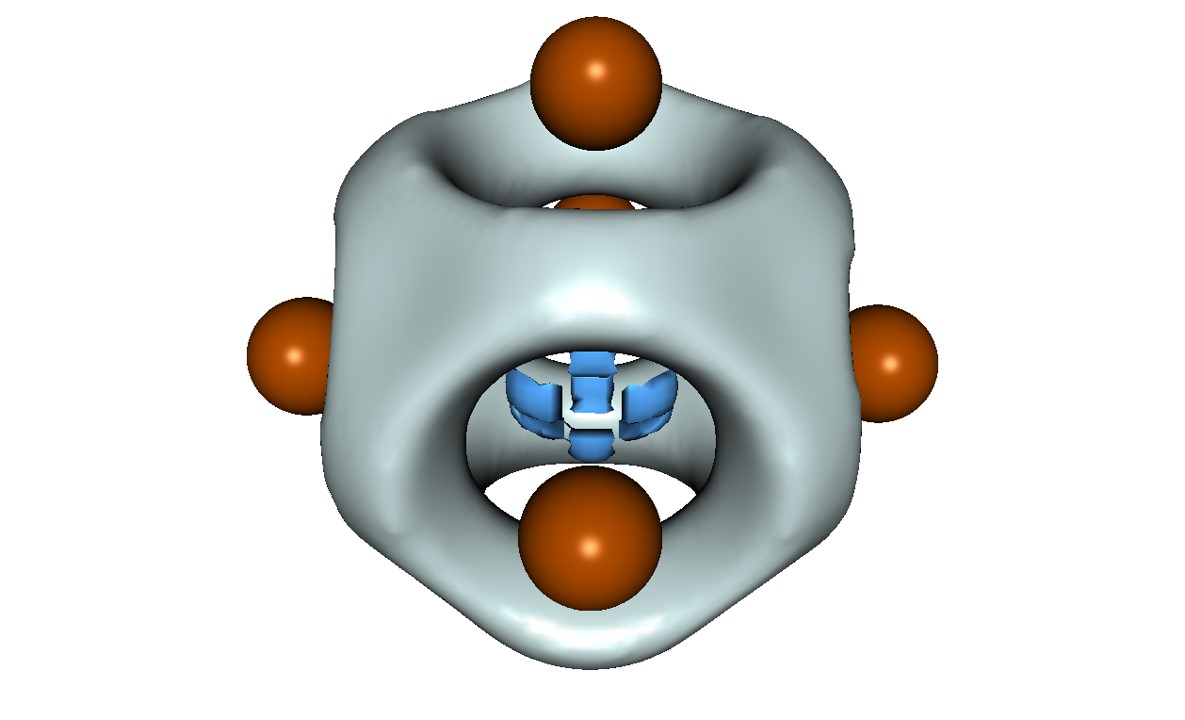
El que mostra el gràfic de l'ELF en aquesta molècula és que tots els electrons de valència de la molècula es troben deslocalitzats enmig dels cations Li+ (cadascun d'ells amb dos electrons interns localitzats). Es tracta, per tant, d'una situació idèntica a la que ens trobem en els metalls. A més, els diferents descriptors d'aromaticitat aplicats indiquen que aquesta molècula és aromàtica. Recordem que la característica principal de les molècules aromàtiques és que presenten una elevada deslocalització electrònica en circuits de dues o tres dimensions. En aquesta molècula la deslocalització té lloc dins del circuit de tres dimensions de simetria octaèdrica format pels cations Li+. Finalment comentar que aquesta molècula presenta una aromaticitat de tipus jellium a capa oberta, un tipus d'aromaticitat descrit molt recentment.
Resumint, el 3/2Li6+ és la primera molècula que presenta un enllaç de tipus metàl·lic, un enllaç típic atribuït de forma exclusiva als cristalls metàl·lics. Aquest treball demostra que l'enllaç metàl·lic no és una característica única dels metalls sinó que en determinats casos es pot trobar també en molècules.





